Il COLLAGENE, una proteina essenziale per la nostra salute, per la nostra mobilità e per il nostro aspetto fisico
È la proteina più abbondante e diffusa nel nostro corpo.
Molecola dalla grande resistenza e flessibilità, il collagene forma la struttura di tutti i tessuti del nostro corpo che ci proteggono e ci permettono di stare in piedi e di muoverci.
Costituisce il 70% del peso secco della cartilagine, il 20% delle ossa, l’85% dei tendini, il 70% dei legamenti, il 75% della pelle e il 6% dei muscoli, oltre ad essere il componente principale del tessuto connettivo, che avvolge e protegge tutti i nostri organi vitali interni.

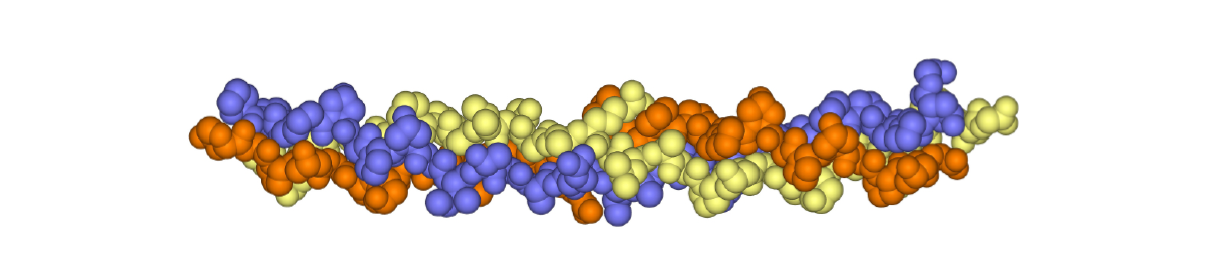
Molecola di collagene
 Dolori articolari
Dolori articolari
 Perdita di massa ossea e decalcificazione ossea che causa fratture
Perdita di massa ossea e decalcificazione ossea che causa fratture



Con il passare del tempo, il nostro collagene si riduce e si deteriora. A partire dai 25 anni ogni anno perdiamo l'1,5% di questa proteina. L’esercizio fisico intenso, oltre che la menopausa e il sovrappeso, accelerano questo processo.
Il collagene è una proteina di origine esclusivamente animale. Allo stato in cui si trova nei tessuti animali (collagene nativo) è una molecola molto lunga e complessa, che non può essere sfruttata come nutriente perché il nostro apparato digerente non è in grado di digerirla e pertanto non la può utilizzare.
Perché questo collagene sia digeribile e assimilabile, è necessario sottoporlo a due processi distinti:
Gelatinizzazione. Separazione della tripla elica della molecola di collagene. Questo processo, attraverso il quale si ottiene la gelatina, viene solitamente eseguito mediante processi chimici (applicazione di alcali o acidi potenti). A differenza degli altri, per la produzione di COLPROPUR D® noi utilizziamo esclusivamente un trattamento fisico (calore).
Idrolisi. Frammentazione delle lunghe catene polipeptidiche di collagene (gelatina) in peptidi (catene corte) mediante enzimi come quelli presenti nell’apparato digerente umano.


Il COLLAGENE IDROLIZZATO è il risultato di questo processo. È composto da peptidi di collagene, molecole abbastanza piccole da poter essere digerite dal nostro apparato digerente, che possono quindi essere utilizzate come nutrienti dal nostro corpo.


Accurati studi scientifici confermano che l’assunzione di 10 grammi al giorno di COLLAGENE IDROLIZZATO (peptidi di collagene bioattivo), facilmente assimilabile, contrasta efficacemente la perdita del collagene, ritardando i sintomi dell’invecchiamento e aiutando a prevenire e trattare le malattie correlate a tale perdita. Il COLLAGENE IDROLIZZATO è il modo più semplice ed efficace per integrare collagene assimilabile nella nostra dieta quotidiana, è una sana abitudine di vita ed è essenziale soprattutto a partire dai 40 anni.
Watanabe-Kamiyama M, Shimizu M, Kamiyama S, et al. “Absorption and effectiveness of orally administered low molecular weight collagen hydrolysate in rats”. J Agric Food Chem 2010; 58(2): 835-41.
Zeijdner E.E. “Digestibility of collagen hydrolysate during passage through a dynamic gastric and small intestinal model (TIM-1) “. TNO Nutrition and food Research Report. 2002, 24 June
Benito-Ruiz P., Villacis R.A., Zurita L.A. et al. “A randomized controlled trial on the efficacy and safety of a food ingredient, collagen hydrolysate, for improving joint comfort”. International Journal of Food Sciences and Nutrition 2009, 60 (S2): 99-113.
Clark K. L., Sebastianelli W., Flechsenhar K. R. et al. “24- week study on the use of collagen hydrolysate as a dietary supplement in athletes with activity-related joint pain”. Current Medical Research and Opinions 2008, 24 (5): 1485-1498.
Gonçalves FK. “Impact of collagen hydrolysate in middle-aged athletes with knee and ankle osteochondral lesions: A case series”. Int J Case Rep Images 2017;8(6):364–369.
Kumar S, Sugihara F, Suzuki K, Inoue N, Venkateswarathirukumara S. “A double-blind, placebo-controlled, randomised, clinical study on the effectiveness of collagen peptide on osteoarthritis” J Sci Food Agric. 2015 Mar 15;95(4):702-7.
Moskowitz, R. W. “Role of Collagen Hydrolysate in Bone and Joint Disease”. Seminars in Arthritis and Rheumatism. 2000; 30 (2): 87-9
Trc T, Bohmova J. “Efficacy and tolerance of enzymatic hydrolysed collagen (EHC) vs. glucosamine sulphate (GS) in the treatment of knee osteoarthritis (KOA)”. Int Orthop.2011; 35:341—8.
Praet, S. et al “Oral Supplementation of Specific Collagen Peptides Combined with Calf-Strengthening Exercises Enhances Function and Reduces Pain in Achilles Tendinopathy Patients”. Nutrients. 2019 Jan 2;11(1).
Daneault, A., et al. “Biological effect of hydrolyzed collagen on bone metabolism” Critical Reviews in Food Science and Nutrition 2017, 57:9, 1922-1937
König D., Oesser S., Scharla S., Zdzieblik D., Gollhofer A. “Specific Collagen Peptides Improve Bone Mineral Density and Bone Markers in Postmenopausal Women—A Randomized Controlled Study” Nutrients 2018, 10, 97
Porfírio E, Fanaro GB. “Collagen supplementation as a complementary therapy for the prevention and treatment of osteoporosis and osteoarthritis: a systematic review” Revista Brasileira de Geriatria e Gerontologia 2016, 19: 153-164
Wauquier, F., et al. “Human Enriched Serum Following Hydrolysed Collagen Absorption Modulates Bone Cell Activity: from Bedside to Bench and Vice Versa” Nutrients 2019, 11, 1249
Asserin J., Lati E., Shioya T., Prawitt J. “The effect of oral collagen peptide supplementation on skin moisture and the dermal collagen network: evidence from an ex vivo model and randomized, placebo-controlled clinical trials” J. of Cosmetic Dermatology 2015, 0, 1–11
Campos, Patrícia Maia, et al. “An oral supplementation based on hydrolyzed collagen and vitamins improves skin elasticity and dermis echogenicity: a clinical placebo-controlled study”. Clin Pharmacol Biopharm 2015, 4: 142
Sibilla S, Godfrey M, Brewer S, Budh-Raja A and Genovese L “An Overview of the Beneficial Effects of Hydrolysed Collagen as a Nutraceutical on Skin Properties: Scientific Background and Clinical Studies” The Open Nutraceuticals Journal, 2015, 8, 29-42 29
Zague, V. et al “Collagen peptides modulate the metabolism of extracellular matrix by human dermal fibroblasts derived from sun-protected and sun-exposed body sites”. Cell Biol Int. 2018 Jan;42(1):95-104.
Jimbo N, Kawada C, Nomura Y. “Optimization of dose of collagen hydrolysate to prevent UVB-irradiated skin damage” Biosci Biotechnol Biochem. 2016;80(2):356-9.
Sugihara F., Inoue N., Venkateswarathirukumara S. “Ingestion of bioactive collagen hydrolysates enhanced pressure ulcer healing in a randomized double-blind placebo-controlled clinical study” Scientific Reports volume 8, Article number: 11403 (2018)
Jendricke, P. et al. “Specific Collagen Peptides in Combination with Resistance Training Improve Body Composition and Regional Muscle Strength in Premenopausal Women: A Randomized Controlled Trial”. Nutrients. 2019 Apr 20;11(4).
Oertzen-Hagemann, V. et al. “Effects of 12 Weeks of Hypertrophy Resistance Exercise Training Combined with Collagen Peptide Supplementation on the Skeletal Muscle Proteome in Recreationally Active Men”. Nutrients. 2019 May 14;11(5).
Olson GB, Savage S, Olson J. 2000. “The effects of collagen hydrolysate on symptoms of chronic fibromyalgia and tempomandibular joint pain”. Cranio, 18(2): 135-41.
Zdzieblik D., Oesser S., Baumstark MW., Gollhofer A., and König D. “Collagen peptide supplementation in combination with resistance training improves body composition and increases muscle strength in elderly sarcopenic men: a randomised controlled trial” British Journal of Nutrition 2015, 114, 1237–1245
Figueres T., Basés E. “Revisión de los efectos beneficiosos de la ingesta de colágeno hidrolizado sobre la salud osteoarticular y el envejecimiento dérmico” Nutrición Hospitalaria, vol. 32, núm. 1, 2015, pp. 62-66
Koyama Y. “Effects of Collagen Ingestion and their Biological Significance” J Nutr Food Sci 2016, 6: 504.
Paul, C. et al. “Significant Amounts of Functional Collagen Peptides Can Be Incorporated in the Diet While Maintaining Indispensable Amino Acid Balance”. Nutrients. 2019 May 15;11(5).
Song H., Li B. “Beneficial Effects of Collagen Hydrolysate: A Review on Recent Developments”. Biomed J Sci &Tech Res 2017, 1(2).